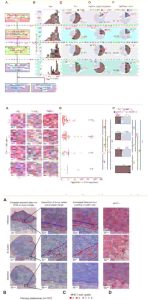
▲ 研究模型:在转移性黑色素瘤中,肿瘤细胞通过下调MHC-I分子使其对CD8+ T细胞“隐形”。同时,免疫抑制性微环境阻碍了T细胞的招募和浸润。这两个过程相互强化,共同导致了对免疫检查点抑制剂(ICI)的原发或获得性耐药。 自2011年首个免疫检查点抑制剂(ICI)获批以来,晚期黑色素瘤的治疗迎来了革命性突破。 然而,临床现实依然严峻:高达40-60%的患者对ICI(如抗PD-1/PD-L1、抗CTLA-4抗体)呈现原发性耐药,而初始应答者中也有相当一部分会经历获得性耐药并最终复发。近日,一项发表于国际权威期刊《Cancer Immunology, Immunotherapy》的研究,通过对大量黑色素瘤患者样本进行系统性分析,揭示了驱动这种耐药性的两大核心且高度协同的生物学特征:1)肿瘤细胞自身主要组织相容性复合物I类(MHC-I)分子的表达显著下调甚至完全缺失;2)肿瘤微环境(TME)中CD8+ 细胞毒性T淋巴细胞(CTLs)的浸润水平严重不足。这两大因素并非孤立存在,而是相互促进,共同构筑了一道坚不可摧的“双重枷锁”,使肿瘤成功逃避免疫系统的监视与清除。本文将深度剖析这一机制,并探讨如何利用前沿技术破局,同时介绍桂芎生物如何赋能相关研究与药物开发。
免疫检查点抑制剂(ICI)在黑色素瘤治疗中的成功,推动了ICI在疾病更早期阶段的应用。这使得许多复发风险较低的患者面临长期不良事件的风险,凸显了开发生物标志物以指导ICI使用的必要性。早在多年前,原发性黑色素瘤中淋巴细胞的活跃浸润就被证实与患者预后改善相关;然而,由于分类系统的高度变异性,相关研究结果存在争议。CD8+ T细胞已被确认为接受ICI治疗的患者抗肿瘤免疫的主要介导者。由于CD8+ T细胞需通过靶细胞上的MHC-I分子呈递抗原,因此MHC-I的下调和缺失已被观察到作为ICI治疗的耐药机制。在本研究中,我们利用自动化免疫组化与数字病理学流程,对一组晚期原发性黑色素瘤及其匹配的转移性黑色素瘤队列进行了回顾性分析,重新探讨了MHC-I表达及CD8+ T细胞浸润在黑色素瘤演变过程中的作用。我们的研究结果显示,MHC-I表达下调是晚期原发性黑色素瘤中常见的现象,且与CD8+ T细胞浸润减少以及向前哨淋巴结的早期转移密切相关。此外,MHC-I表达下调和CD8+ T细胞浸润减少还与ICI治疗的耐药性相关。这些发现提示,未来可将MHC-I表达水平及CD8+ T细胞浸润模式的分析用作生物标志物,以指导在黑色素瘤早期阶段采用ICI治疗的决策。
免疫检查点抑制剂(ICI)针对CTLA4和PD1受体的引入,彻底改变了晚期黑色素瘤患者的治疗方式,并凸显了T细胞在控制肿瘤生长中的重要作用。 ICI在转移性疾病中的成功应用,推动了其在疾病更早期阶段的广泛应用,2022年ICI获批用于IIB至IIC期黑色素瘤便是这一趋势的典型体现。由于早期患者复发风险较低,与晚期患者相比,接受辅助治疗获益的早期患者比例较小,而不良事件的风险却基本相当。 这凸显了开发新型生物标志物以指导治疗决策的迫切需求。
早在ICI被纳入常规临床诊疗之前,人们就已发现黑色素瘤的发生与发展与淋巴细胞浸润之间存在关联。多年前,皮肤病理学家便经常观察到侵袭性黑色素瘤中存在淋巴细胞浸润,而在良性黑素细胞痣中则极为少见。5 肿瘤浸润淋巴细胞(TIL)的模式最初被划分为三类:「活跃」、「不活跃」和「缺失」。6 在一组I期和II期黑色素瘤患者中,肿瘤浸润呈「活跃」的患者显示出更长的总生存期(OS),而浸润模式为「不活跃」或「缺失」的患者则生存期较短。此后,又出现了更多分类系统,国际免疫肿瘤学生物标志物工作组也尝试对TIL分类进行标准化。对这些不同分类系统的比较研究得出了颇具争议的结论,这可能源于染色和分析方法上的差异。此外,基于形态学的TIL评估无法区分不同的淋巴细胞亚群。这些问题限制了病理学TIL分级作为常规临床诊疗生物标志物的实用性。
CD8+ T细胞已被证实是ICI增强抗肿瘤免疫的主要贡献者。 为了成功地对肿瘤细胞发起免疫攻击,CD8+ T细胞必须识别靶细胞上由MHC-I分子呈递的抗原。 正如MHC-I在CD8+ T细胞介导的抗肿瘤免疫中所发挥的关键作用,研究发现,在黑色素瘤的癌症进展过程中,MHC-I功能的破坏已成为一种免疫逃逸策略。 此外,早期的研究还报道,作为对黑色素瘤过继细胞疗法免疫治疗产生耐药性的机制之一,MHC-I分子的重要组成部分β2微球蛋白出现了缺失现象。 类似地,黑色素瘤细胞中MHC-I表达的下调也被确认为对ICI治疗产生耐药性的机制之一,这凸显了CD8+ T细胞介导的免疫反应对于ICI疗效的重要性。 尽管MHC-I介导的抗原呈递对于有效抗肿瘤免疫的重要性已得到充分证实,但在肿瘤演进早期MHC-I下调的发生频率和时间却仍 largely 不明。 过去几十年的技术进步显著拓展了组织病理学分析的方法学手段。最初,免疫组织化学(IHC)染色需要使用冷冻切片,并且完全依靠手工操作。如今,自动化染色设备与合适的单克隆抗体使得即使在福尔马林固定、石蜡包埋的组织切片上也能实现可重复的IHC分析。 此外,全切片扫描仪的引入将整个切片图像数字化,推动了数字病理算法的发展,进一步提高了图像分析的可重复性。在本研究中,我们旨在利用现代自动化IHC染色技术和数字病理学工具,探究MHC-I在真实世界黑色素瘤患者队列中肿瘤演进过程中的下调频率与时间特征。我们比较了原发肿瘤、早期转移灶以及免疫治疗后复发的转移灶,并将MHC-I的表达水平与CD8+ T细胞浸润模式相关联。我们假设,在肿瘤演进早期评估MHC-I表达水平及T细胞浸润模式,可能成为潜在的生物标志物,有助于指导日常临床诊疗中的治疗决策。
第一章:免疫识别的基石——MHC-I为何至关重要?
要理解这项研究的意义,首先必须回顾T细胞介导的适应性免疫应答的基本原理。CD8+ T细胞是机体清除病毒感染细胞和肿瘤细胞的主力军。其杀伤功能的启动,依赖于一个精密的“三元识别”过程:
- 抗原加工与呈递
肿瘤细胞内的异常蛋白(如突变产生的新抗原)被蛋白酶体降解成短肽(通常8-11个氨基酸),这些肽段被转运至内质网,与新合成的MHC-I分子结合,形成稳定的pMHC-I复合物。 - 表面展示
pMHC-I复合物被转运至细胞膜表面,如同一个“身份标签”,向巡逻的T细胞展示其内部状态。 - TCR特异性识别
CD8+ T细胞通过其表面的T细胞受体(TCR)特异性地识别这个“身份标签”。一旦识别成功,CD8共受体(结合MHC-I的α3结构域)会提供关键的稳定化信号和Lck激酶活性,共同触发T细胞的激活、增殖和效应功能(如释放穿孔素、颗粒酶)。
因此,MHC-I分子是连接肿瘤内在异常与外在免疫监视的桥梁。如果这座桥梁被破坏,再强大的T细胞也无法“看见”肿瘤。
第二章:“双重枷锁”的形成:从研究发现到机制解析
该研究团队收集了涵盖原发灶、不同部位转移灶以及接受ICI治疗前后的黑色素瘤组织样本,并运用了包括多重免疫荧光(mIF)、流式细胞术、RNA测序和数字病理学在内的多种先进技术进行综合分析。
核心发现一:MHC-I下调是转移和耐药的普遍特征研究发现,与原发肿瘤相比,转移性病灶中的肿瘤细胞表现出更高频率和更大幅度的MHC-I(特别是经典的HLA-A、-B、-C亚型)表达下调。这种下调在ICI治疗无应答的患者队列中尤为显著。机制上,这可能源于多种原因:
- 基因层面
B2M(β2-微球蛋白)基因的失活突变或缺失,这是MHC-I复合物组装所必需的。 - 表观遗传层面
MHC-I基因启动子区域的甲基化导致转录沉默。 - 信号通路层面
JAK/STAT、NLRC5等调控MHC-I表达的关键通路发生功能障碍。 - 微环境压力
长期暴露于炎症因子(如TNF-α)可能导致MHC-I的内化或降解。
核心发现二:CD8+ T细胞浸润与MHC-I状态紧密耦合通过空间分辨的mIF技术,研究者观察到一个清晰的模式:在MHC-I高表达的肿瘤区域,通常能检测到密集的CD8+ T细胞浸润,形成所谓的“免疫炎症型”(Inflamed)或“热肿瘤”表型。相反,在MHC-I低/无表达的区域,T细胞要么完全缺席(“免疫沙漠型”),要么被限制在肿瘤边缘无法进入实质(“免疫排斥型”)。
核心发现三:二者形成自我强化的恶性循环这两个过程并非简单的因果关系,而是构成了一个动态的、自我强化的免疫逃逸回路:正向循环:MHC-I缺失 → T细胞无法识别 → T细胞不被招募/激活 → T细胞浸润减少 → 缺乏T细胞来源的IFN-γ → IFN-γ信号通路无法激活 → MHC-I表达进一步下调。负向循环(理想状态):MHC-I高表达 → T细胞有效识别并杀伤 → 释放IFN-γ → IFN-γ刺激肿瘤细胞上调MHC-I和其他抗原加工呈递机器(APM)组分 → 增强免疫原性 → 吸引更多T细胞浸润。
在耐药的黑色素瘤中,前者占据了主导地位,使得ICI(旨在解除T细胞的“刹车”)因缺乏可被激活的“引擎”(即能识别肿瘤的T细胞)而失效。
第三章:破局之道——超越PD-1/PD-L1的下一代策略
面对这“双重枷锁”,研发策略必须从单一靶点转向多维度、组合式的干预。目前主要有三大方向:
-
面对这“双重枷锁”,研发策略必须从单一靶点转向多维度、组合式的干预。目前主要有三大方向:
1、恢复MHC-I表达通路表观遗传调节剂 :
- DNA甲基转移酶抑制剂(DNMTi)或组蛋白去乙酰化酶抑制剂(HDACi),可逆转MHC-I基因的沉默状态。
- IFN-γ通路激动剂:直接激活JAK/STAT通路,强力诱导MHC-I和APM组分的表达。
- 靶向负调控因子:开发抑制MHC-I内化或降解通路的小分子药物。
2、开发MHC-I非依赖性免疫疗法NK细胞疗法:
- NK细胞通过“Missing-self”机制识别并杀伤MHC-I低表达的细胞,是天然的“MHC-I缺失”肿瘤杀手。
- T细胞衔接器(TCE):双特异性抗体,一端结合肿瘤表面的非MHC抗原(如GD2, B7-H3),另一端结合T细胞的CD3,强制激活T细胞杀伤,完全绕过TCR-pMHC识别。
- CAR-T/NK细胞:通过工程化赋予T/NK细胞识别特定肿瘤抗原的能力,同样不依赖于MHC-I。
3、精准分层与理性联合治疗在治疗前对患者的肿瘤进行“免疫画像”(Immune Profiling),根据其MHC-I状态和TILs浸润情况,选择最匹配的疗法。例如:
- MHC-I完整 + T细胞浸润不足:ICI + 促进T细胞浸润的药物(如溶瘤病毒、STING激动剂)。
- MHC-I缺失 + T细胞存在:NK细胞疗法或TCE。
- MHC-I缺失 + T细胞缺失:可能需要先用药物恢复MHC-I,再联合ICI或其他疗法。
结语:从机制洞察到临床转化
这项关于黑色素瘤“双重枷锁”的研究,是肿瘤免疫学从现象描述走向机制深挖的典范。它告诉我们,成功的免疫治疗不再是“一刀切”的模式,而是建立在对每个患者肿瘤独特免疫景观的深刻理解之上。
对于药物开发者而言,这意味着我们必须在临床前阶段就充分考虑MHC-I状态这一关键变量。无论是开发旨在恢复MHC-I的药物,还是开发绕过MHC-I的新一代细胞疗法,都需要一个能够精确模拟和评估这一复杂生物学场景的技术平台。
**桂芎生物的使命,正是成为您在这条充满挑战但前景光明的道路上最值得信赖的科学伙伴**。 我们的综合技术平台,能够帮助您从分子、细胞、组织空间乃至功能等多个维度,全面解码肿瘤的免疫逃逸密码,为您的创新疗法提供从靶点发现、机制验证到IND-enabling研究的全链条、高质量支持。
因为,只有真正理解了“枷锁”是如何形成的,我们才能锻造出打开它的那把最锋利的“钥匙”。
参考文献:Downregulation of MHC-I on Melanoma Cells and Decreased CD8+ T-Cell Infiltration Are Associated With Metastatic Spread and Resistance to Immunotherapy. Lab Invest . 2025
如何将“数字化响应”转化为实验或产品?
若您正开展以下工作,桂芎生物可提供关键技术支撑:
1. 微量pMHC复合物合成服务: 支持HLA-A*02:01等主流等位基因,用于抗原特异性T细胞验证
2 . pMHC荧光四聚体合成以及筛选: 现货覆盖多种肿瘤抗原(如CMV/EBV/KRAS等),快速分选抗原特异性T细胞
3. 工程化呈递细胞构建: K562-HLA系列,模拟体内抗原呈递,用于DC功能模拟
4. 单克隆TCR测序: 从四聚体阳性T细胞中获取配对链的TCR主克隆
5. 抗原肽-MHC亲和力高通量ELISA扫描服务: 高通量筛选最优表位,指导DC疫苗设计
6. 抗原特异性T细胞扩增: 桂芎拥有稳定的抗原特异性DC的分化成熟工艺,是抗原特异性T细胞扩增和检测的基石。
点击网页右侧”快速联系人“扫码,获取服务方案 + 成功案例.
Views: 25