💡 树突状细胞(DCs),被誉为免疫系统的“全能指挥官”,不仅能精准识别病原体与异常细胞,还能调动T细胞和B细胞发起攻击。从癌症到糖尿病,从感染性疾病到自身免疫病,DCs正引领一场全新的治疗革命!
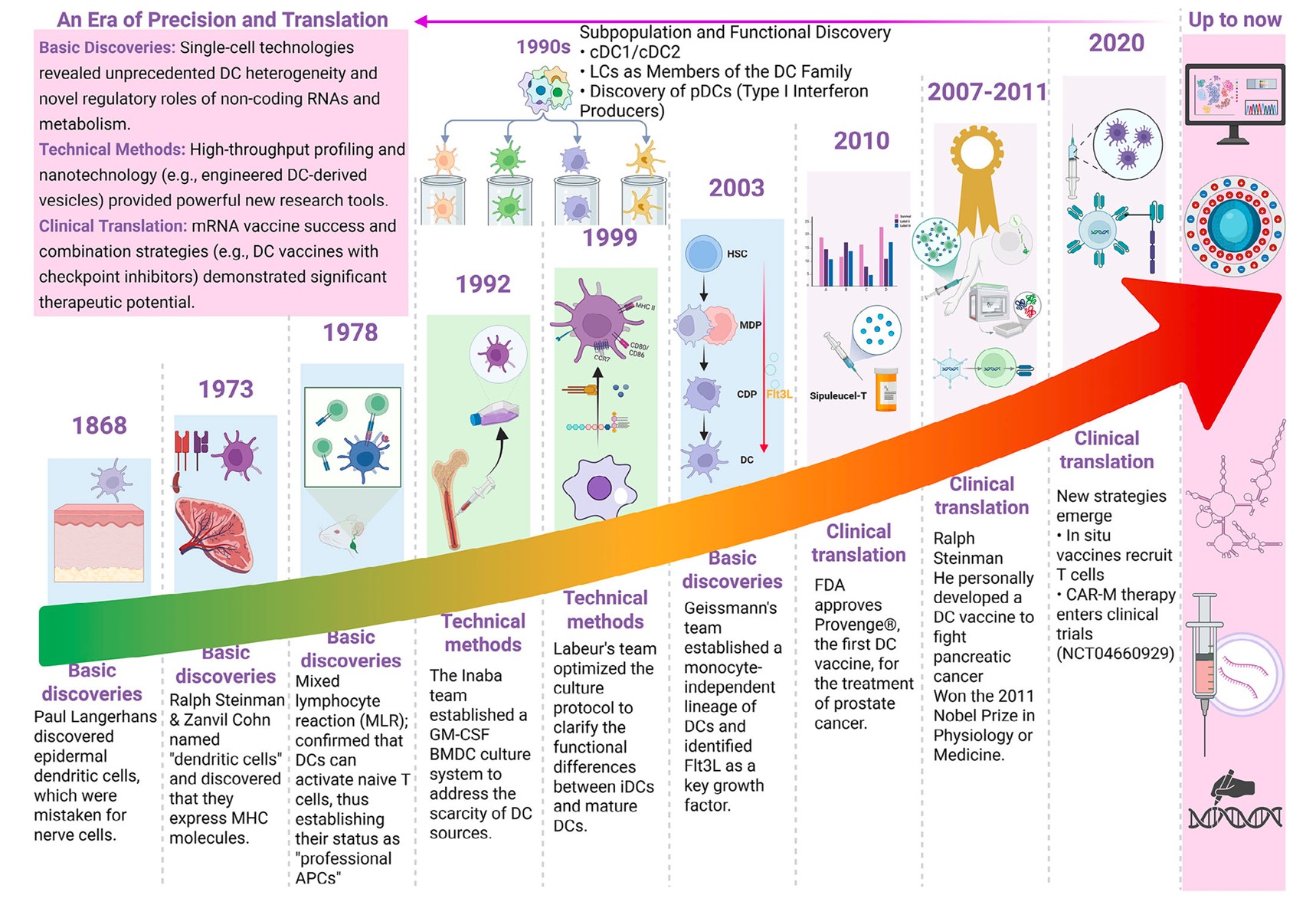
DC研究里程碑(参考文献来源:Dendritic Cells: Origin, Classification, Development, Biological Functions, and Therapeutic Potential)
一、初识DCs:免疫网络的核心枢纽
1973年,拉尔夫·斯坦曼首次发现了树突状细胞(DCs)。作为专业的抗原提呈细胞(APCs),DCs是连接先天免疫与适应性免疫的关键桥梁。它们在外周组织中捕获抗原后,迁移到淋巴器官,将抗原信息传递给T细胞和B细胞,启动针对性免疫应答。
- cDC1s:擅长交叉提呈肿瘤抗原,激活细胞毒性T细胞;
- pDCs:大量分泌I型干扰素,在抗病毒中发挥关键作用;
- LCs:坚守皮肤等上皮组织,构成免疫第一道防线。
二、DCs的“全能技能”:从免疫激活到耐受调节
抗原处理与提呈
DCs通过巨胞饮、吞噬作用和受体介导内吞等方式捕获抗原,将其降解为肽段后,通过MHCⅠ类分子提呈给CD8⁺T细胞,或通过MHCⅡ类分子提呈给CD4⁺T细胞。尤为特殊的是“交叉提呈”能力——cDC1s可将外源性抗原通过MHCⅠ类分子提呈,激活细胞毒性T细胞。
免疫激活
DCs通过“三信号机制”启动适应性免疫:T细胞受体识别抗原-MHC复合物(第一信号),CD80/CD86与CD28结合提供共刺激信号(第二信号),DCs分泌IL-12、IFN等细胞因子引导T细胞分化(第三信号)。这一过程可激活CD4⁺T细胞分化为Th1、Th2、Th17等效应亚群,CD8⁺T细胞分化为细胞毒性T细胞,同时促进B细胞产生抗体。
免疫调节
DCs不仅能启动免疫攻击,还能通过中枢耐受(胸腺中清除自身反应性T细胞)和外周耐受(诱导调节性T细胞)避免免疫过度激活。当转化为tolDCs时,会通过分泌IL-10、TGF-β等抑制性细胞因子,维持机体免疫平衡。
三、疾病治疗的“新武器”:DCs的临床应用突破
(一)癌症免疫治疗:从疫苗到联合疗法
DC疫苗通过加载肿瘤抗原,激活机体自身抗肿瘤免疫。首个获批的前列腺癌疫苗Provenge(sipuleucel-T)可延长患者中位生存期4.1个月。如今,DC疫苗已发展出多种形式:肽负载疫苗、基因工程疫苗、个性化新抗原疫苗等。
-
黑色素瘤、肝癌、胰腺癌等多种癌症的临床试验显示,DC疫苗能有效激活肿瘤特异性T细胞; -
联合治疗策略如DC疫苗与免疫检查点抑制剂联用,显著提升疗效。
(二)代谢性疾病:重塑免疫代谢平衡
在1型糖尿病(T1DM)中,DCs呈递胰岛β细胞自身抗原,导致β细胞损伤。通过维生素D₃、雷帕霉素等修饰DCs,可诱导免疫耐受,保护胰岛功能。临床研究显示,胰岛素肽脉冲的tolDCs能稳定T1DM患者的血糖控制。
(三)感染性疾病:对抗病原体的“免疫增强剂”
DCs通过TLR受体识别病毒、细菌等病原体的PAMPs,启动针对性免疫应答。自体DC疫苗在慢性HIV感染中可降低病毒载量,扩增HIV特异性T细胞;针对COVID-19的DC疫苗,能诱导强效T细胞免疫,保护率达95.56%。
(四)自身免疫病与移植:诱导免疫耐受
DCs可通过诱导调节性T细胞、分泌抑制性细胞因子,抑制病理性免疫反应。在器官移植中,DCs既能促进移植排斥,也能诱导免疫耐受——通过基因工程改造或药物修饰DCs,可延长移植物存活时间。
四、桂芎生物:赋能DC疗法创新开发
要复现或超越上述临床成果,您需要:高纯度抗原肽 + pMHC四聚体 + 工程化APC构建。桂芎生物已构建完整平台:
1. 抗原特异性T细胞扩增: 桂芎拥有稳定的抗原特异性DC的分化成熟工艺,是抗原特异性T细胞扩增和检测的基石。
2. 微量pMHC复合物合成服务: 支持包括HLA-A*02:01等30多种HLA亚型的pMHC,用于DC功能验证
3. pMHC荧光四聚体合成以及筛选: 现货覆盖多种肿瘤抗原(如CMV/EBV/KRAS等),快速分选抗原特异性T细胞
4. 单克隆TCR测序: 从四聚体分选抗原特异性T细胞中配对TCR主克隆
5. 抗原肽-MHC亲和力高通量ELISA扫描服务: 高通量筛选最优新抗原表位,指导DC疫苗设计
7. 工程化呈递细胞构建: K562-HLA系列,模拟体内抗原呈递,用于DC功能验证
五、应用场景建议
-
癌症DC疫苗开发:用四聚体分选T细胞,建立临床cut-off值; -
个性化新抗原疫苗:基于NGS技术设计精准抗原; -
感染性疾病DC疫苗:通过加载病原体抗原,诱导强效T细胞免疫; -
自身免疫病tol-DCs疗法:通过修饰DCs,诱导免疫耐受。
Views: 16
