TCR-T细胞治疗全流程:从肿瘤抗原发现 → TCR克隆 → 基因工程 → 功能验证 → 临床回输 TCR-T细胞疗法通过将高亲和力肿瘤特异性TCR基因导入患者T细胞,赋予其精准识别MHC-呈递肿瘤抗原的能力。与CAR-T不同,TCR-T可靶向胞内抗原,在实体瘤治疗中具有不可替代的优势,但其成功高度依赖于抗原加工与MHC递呈的完整性。
一、TCR-T细胞的精确定义与作用原理
TCR-T细胞是指通过病毒载体(如慢病毒、逆转录病毒)或非病毒方法(如转座子、mRNA电转)将编码特定αβ TCR的基因导入自体外周血T细胞后获得的工程化T细胞。其核心特征包括:
- 抗原特异性:
由外源TCR决定,通常来源于肿瘤浸润淋巴细胞(TILs)、疫苗应答者或健康供体中的高亲和力克隆; - MHC限制性:
必须识别由特定HLA等位基因(如HLA-A*02:01)呈递的8–10 aa肽段; - 信号依赖宿主通路:
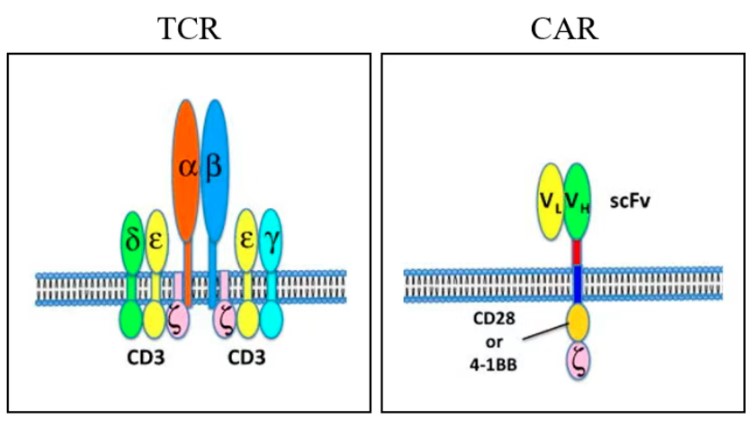
TCR本身无胞内信号域,需与内源CD3复合物(CD3εδ/εγ/ζζ)组装才能启动Zap-70磷酸化级联; - 共受体协同:
CD8⁺ TCR-T细胞依赖CD8αβ结合MHC I的α3结构域,提升pMHC驻留时间约10倍(KD从μM级改善至nM级)。
与CAR-T的关键区别(见下表):
|
|
|
|
|---|---|---|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
二、抗原递呈:TCR-T识别的分子基础
TCR-T能否有效杀伤肿瘤,取决于靶细胞是否能将肿瘤相关抗原(TAA)或新抗原(NeoAg)正确加工并呈递于MHC I类分子表面。该过程涉及多个精密调控的生化步骤。
1. 内源性抗原的MHC I类递呈通路(经典途径)
这是TCR-T识别实体瘤的主要通路,具体步骤如下:
- 蛋白酶体降解:肿瘤细胞内异常蛋白(如突变p53、NY-ESO-1)被泛素化标记,送入26S蛋白酶体降解为5–25 aa肽段;
- TAP转运:肽段在Hsp70/Hsp90协助下,经抗原加工转运体(TAP1/TAP2异源二聚体)从胞质转运至内质网(ER)腔。TAP偏好8–16 aa、C端疏水/碱性残基的肽段;
- MHC I组装:在ER中,新生MHC I重链(α链)与β₂m结合,并在伴侣蛋白(calnexin → calreticulin/ERp57)辅助下形成“肽装载复合物”(PLC),包含TAP、tapasin等;
- 肽选择与稳定:仅与MHC I结合槽匹配良好的肽(通常8–10 aa,含锚定残基如P2/P9)被保留,其余被ERAP1/2进一步修剪或降解;
- 表面呈递:稳定pMHC I复合物经高尔基体转运至细胞膜,密度通常为10³–10⁵ copies/cell。
临床警示:许多肿瘤通过下调TAP、β₂m或MHC I表达逃避免疫监视,导致TCR-T失效。因此,治疗前需检测靶细胞MHC I表达水平。
2. 外源性抗原的MHC II类递呈(对CD4⁺ TCR-T的意义)
虽然多数TCR-T基于CD8⁺ T细胞,但近年研究发现,CD4⁺ TCR-T可通过识别MHC II-呈递的肿瘤抗原(如MAGE-A3、WT1)提供长效免疫记忆和辅助功能。
-
抗原被树突状细胞(DC)吞噬 → 形成早期内体 → 酸化成熟为晚期内体/溶酶体; -
蛋白酶(cathepsins)降解抗原为13–25 aa肽段; -
MHC II在ER中与恒定链(Ii)结合,防止提前结合肽;进入内体后,Ii被降解,仅留CLIP片段; -
H2-DM催化CLIP替换为抗原肽,形成pMHC II复合物,转运至表面供CD4⁺ T细胞识别。
3. 非经典递呈途径:交叉呈递(Cross-presentation)
树突状细胞可将外源性肿瘤抗原(如凋亡小体、外泌体)通过MHC I呈递给CD8⁺ T细胞,这一过程称为交叉呈递。其机制包括:
- 液泡途径:抗原在内体中直接加载至MHC I;
- 胞质途径:抗原从内体逃逸至胞质,进入经典MHC I通路。
此机制对启动初始T细胞应答至关重要,也是DC疫苗联合TCR-T治疗的理论基础。
三、TCR-T靶点选择的关键考量
理想的TCR-T靶点需满足以下条件:
- 肿瘤特异性:优先选择新抗原(NeoAg)或癌睾抗原(如NY-ESO-1、MAGE-A4),避免攻击正常组织;
- 高表达与稳定呈递:靶抗原在肿瘤中高表达,且加工通路完整(TAP⁺/MHC I⁺);
- HLA覆盖广:优选中国人群高频HLA等位基因(如HLA-A*02:01, *11:01, *24:02)对应的表位;
- 免疫原性强:能诱导高亲和力TCR(KD < 10 μM),且无中枢耐受。
历史教训:2009年一项MAGE-A3 TCR-T临床试验因TCR交叉识别脑组织中MAGE-A12导致2例患者死亡,凸显脱靶毒性风险。
桂芎生物:支撑TCR-T研发全链条的技术平台
针对上述关键环节,桂芎提供以下深度技术服务:
1. 抗原特异性T细胞扩增:桂芎特有的DC分化成熟流程,提供高比例CD83/CD86呈递细胞,体外扩增高纯度Tfh/CD8⁺ T细胞克隆
2. 微量pMHC复合物合成服务:支持低至μg级定制,适用于小鼠/人源HLA等位基因
3. pMHC荧光四聚体合成以及筛选:现货2000+种,覆盖HLA-A*02:01/A*11:01/A*24:02等30多种主流HLA亚型基因
4. 单克隆TCR测序: 从分选T细胞中获取配对全长TCRα/β主克隆
5. 稳转原代TCR-T构建: 整合murine TCR恒定区的非病毒TCR稳转系统,更安全的临床前研究应用
6. 抗原肽-MHC亲和力高通量ELISA扫描服务: 高通量评估数百种肽段与HLA结合能力,优选疫苗表位
7. 工程化呈递细胞构建: K562-HLA系列细胞,用于持久抗原呈递
Views: 55
