TCR与pMHC的相互作用发生在原子尺度。理解其动态行为,是设计高亲和力、高特异性TCR-T疗法的关键。 在TCR-T细胞疗法进入临床爆发期的今天,一个核心挑战依然存在:如何从海量候选TCR中,快速、精准地筛选出那些既能强力结合肿瘤新抗原、又不会误伤正常组织的“黄金TCR”?答案,或许就藏在十年前的一篇被低估的综述里。2015年,牛津大学Charlotte Deane团队在《Briefings in Bioinformatics》上发文Current status and future challenges in T-cell receptor/peptide/MHC molecular dynamics simulations,系统梳理了利用分子动力学(MD)模拟研究TCR/肽/MHC(pMHC)复合物的现状与未来。这篇论文(PMID: 25725219)不仅是一份技术报告,更是一张精准的路线图,预言了今日TCR理性设计所依赖的计算革命。
第一章:为何静态结构不足以揭示免疫识别的真相?
T细胞通过其表面的T细胞受体(TCR)来扫描由MHC-I分子呈递的抗原肽(即pMHC)。传统X射线晶体学为我们提供了高分辨率的复合物“快照”,但这些结构往往是能量最低、最稳定的构象。
然而,真实的免疫识别是一个**高度动态的过程**。TCR与pMHC的结合涉及:
- 柔性诱导
肽段和TCR的互补决定区(CDR)环会发生构象调整; - 水分子介导
界面水分子网络的形成与解离对结合能至关重要; - 瞬时相互作用
氢键、盐桥、范德华力等在纳秒尺度上不断形成与断裂。
这些**毫秒甚至纳秒级别的细微动态**,恰恰决定了TCR结合的亲和力、交叉反应性和最终的T细胞激活效率。而这些信息,是静态结构无法提供的。
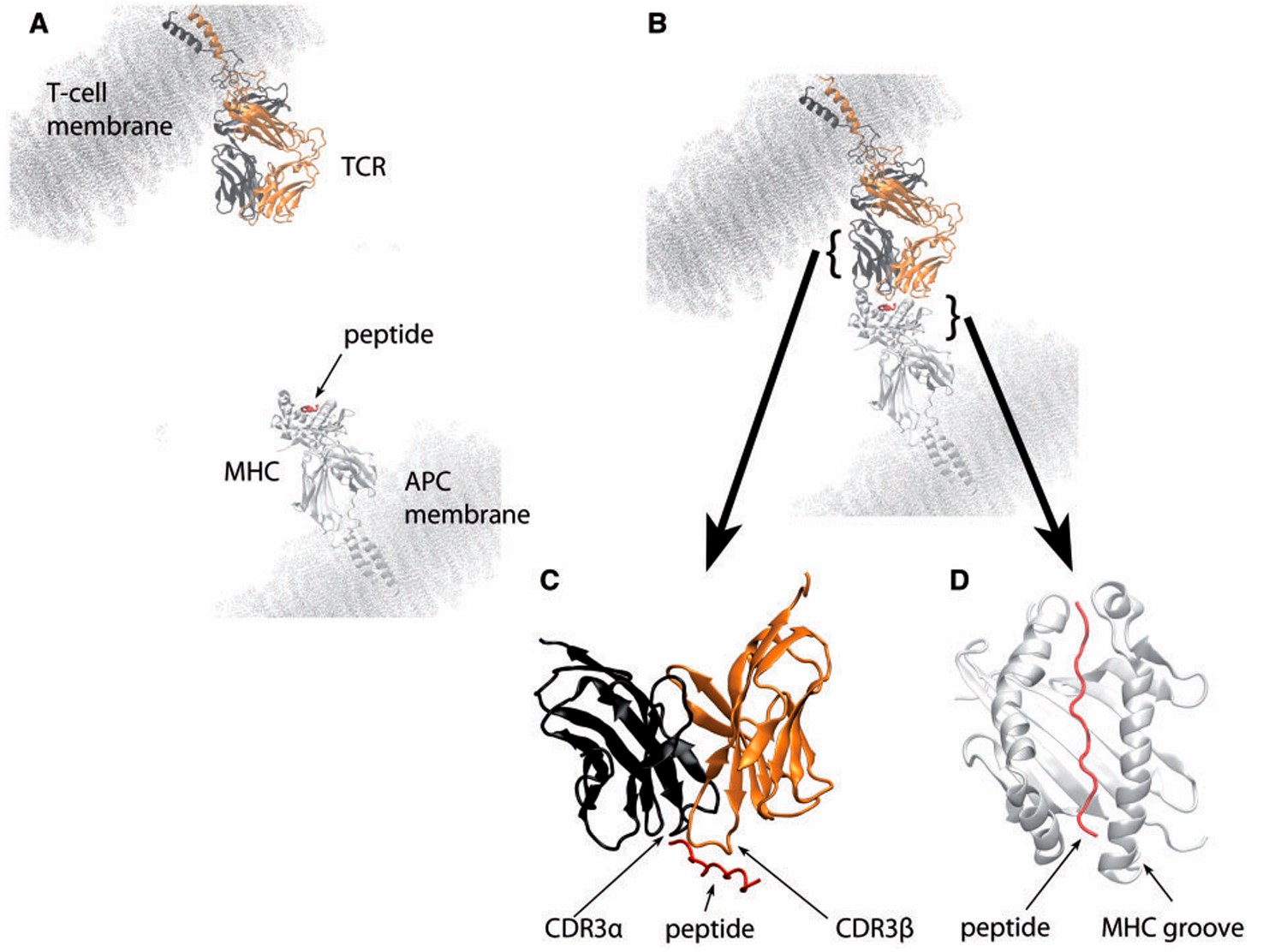
第二章:2015年的全景图——方法、洞见与核心挑战
Knapp等人在综述中系统性地总结了当时的研究范式,并指出了三大关键挑战:
更重要的是,作者敏锐地指出:**TCR-pMHC的相互作用模式具有高度多样性**。不存在一个放之四海而皆准的“通用模型”,必须针对每个特定的复合物进行细致分析。
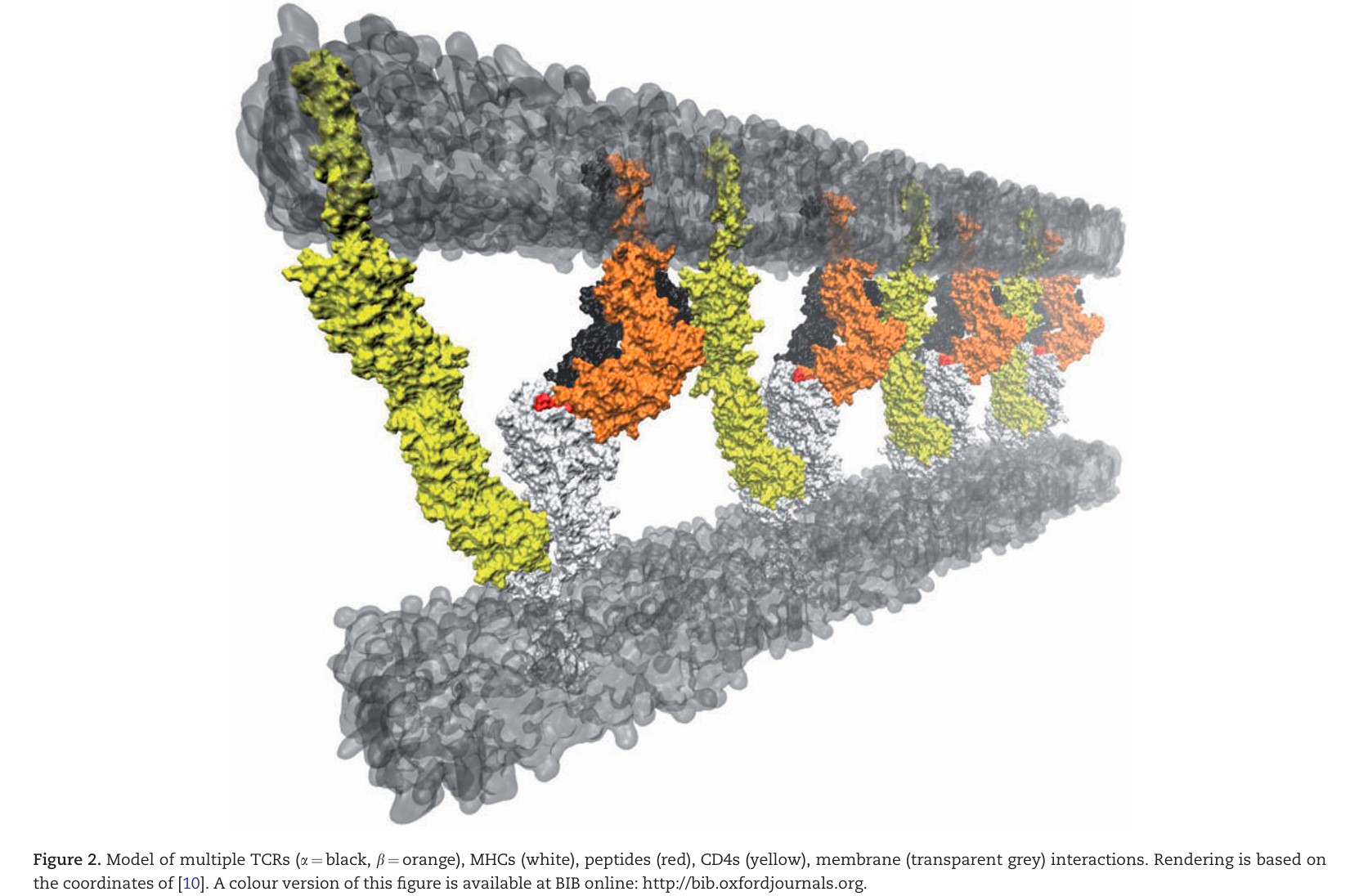
第三章:十年跨越——从挑战到解决方案
回望过去十年,综述中提出的挑战正被一一攻克:
- AI驱动的结构预测
AlphaFold2和RoseTTAFold的出现,极大提升了TCR-pMHC复合物初始模型的准确性,为后续MD模拟奠定了坚实基础。 - 算力革命
GPU集群和专用硬件(如Anton)将模拟时长推进至微秒乃至毫秒级别,足以观察到功能相关的慢速动力学过程。 - 增强采样算法
元动力学(Metadynamics)、副本交换(REMD)等方法能有效跨越能量壁垒,探索更广阔的构象空间。 - 多尺度建模
从全原子MD到粗粒化模型,再到机器学习势函数,形成了覆盖不同时间和空间尺度的完整工具链。
如今,MD模拟已不再是纯粹的学术探索,而是**TCR亲和力成熟、特异性评估和脱靶风险预测**的核心环节。
结语:站在巨人的肩膀上,走向精准免疫治疗的未来
Knapp等人的这篇综述,如同一座灯塔,在TCR计算生物学的早期迷雾中指明了方向。它告诉我们,要真正驾驭T细胞的识别能力,就必须深入到原子运动的层面。
今天,随着实验技术与计算科学的深度融合,我们已经能够构建一个“**发现-验证-优化**”的完整闭环。桂芎生物正是这一趋势的践行者,致力于将最前沿的科学洞见,转化为攻克癌症的有力武器。
从十年前的一篇综述,到今天拯救生命的疗法,这正是基础科学研究最动人的力量。
桂芎生物:提供抗原特异性T细胞全链条解决方案
1. 抗原特异性T细胞扩增: 覆盖黑色素瘤核心抗原(MART-1/gp100/NY-ESO-1等),支持HLA-A*02:01等主流等位基因
2. 微量pMHC复合物合成服务: 快速定制,少量验证,同步追踪多个抗原特异性T细胞克隆
3. pMHC荧光四聚体合成以及筛选: 基于四聚体分选细胞,扩增高纯度T-bet⁺功能性T细胞
4. 单克隆TCR测序: 从四聚体分选抗原特异性T细胞中配对TCR主克隆
5. 稳转原代TCR-T构建: 整合murine TCR恒定区的非病毒TCR稳转系统,更安全的临床前研究应用
6. 抗原肽-MHC亲和力高通量ELISA扫描服务: 高通量筛选最优新抗原表位,指导肽段筛选
7. 工程化呈递细胞构建: K562-HLA系列,模拟体内抗原呈递,用于TCR功能验证
Views: 10
