▲ 研究揭示,MHC-I分子并非刚性结构,其内在的“可塑性”(柔性)决定了它筛选高亲和力抗原肽的能力。B*4405(右)比B*4402(左)更具柔性,因此能更高效地呈递肿瘤抗原。 为什么有些人的免疫系统能有效识别并清除癌细胞,而有些人却不能? 答案可能就藏在我们细胞表面的“告示牌”——MHC-I分子的细微差别里。近日,一项发表于《Scientific Reports》(Nature旗下)的研究,通过结合计算建模、分子动力学模拟和生化实验,首次从原子层面揭示了MHC-I分子的内在“柔性”(Protein Plasticity)是其发挥抗原选择功能的核心密码。这项研究不仅解释了免疫应答个体差异的根源,更为优化癌症疫苗和T细胞疗法提供了全新的设计思路。
谜题:仅一个氨基酸之差,天壤之别的免疫效果
MHC I分子具有高度多态性,但其三级结构却十分相似(图1),主要包括:多态性的重链、单态的β2微球蛋白(β2m)以及一条通常由8至10个氨基酸组成的肽段。这些组分以非共价键的形式结合于肽段结合槽中。当辅助因子分子tapasin功能缺失或不存在时,不同等位基因型MHC I分子在肽段选择功能上的内在差异便会凸显出来。这是因为tapasin能够通过优先增强那些肽段选择效率较低的MHC I分子的选择功能,从而掩盖这些内在差异。而在tapasin缺失的情况下,MHC I分子一级序列中的差异便足以显著影响其肽段选择功能12。例如,两种人类等位基因HLA-B35:01和HLA-B52:01的一级序列仅相差12个氨基酸残基。在缺乏tapasin的情况下,HLA-B35:01分子会在细胞表面高水平表达,而HLA-B52:01分子则仅以低水平存在。值得注意的是,即使仅仅一个氨基酸的差异也能改变MHC I分子的固有肽段选择功能:HLA-B44:02(B4402)与HLA-B44:05(B4405)在第116位仅相差一个氨基酸残基(图1A),然而,在缺乏tapasin的情况下,二者在选择高亲和力肽段的能力上却处于截然相反的两端。在tapasin缺陷的细胞中,B4402难以有效采样肽段库,因此在内质网(ER)中被降解;而B4405则能高效地选择高亲和力肽段,并将其呈递到细胞表面。
研究聚焦于两个人类MHC-I等位基因:HLA-B*44:02 (B*4402) 和 HLA-B*44:05 (B*4405)。它们的蛋白质序列**仅在第116位有一个氨基酸不同**(B*4402是天冬氨酸D,B*4405是酪氨酸Y)。
然而,这个微小的差异却导致了巨大的功能鸿沟:
- B*4405
在没有辅助分子tapasin的帮助下,也能高效地从成千上万的肽段中筛选出高亲和力的抗原肽,并稳定地呈递到细胞表面,让T细胞“看得见”。 - B*4402
自身筛选能力极差,若无tapasin帮助,大部分会因未能结合稳定肽段而在内质网中被降解,导致细胞表面几乎“空空如也”,T细胞无法识别。
这个现象引出了一个根本问题:**静态的晶体结构几乎完全相同(RMSD仅0.3Å),为何功能却如此迥异?**
核心发现:MHC-I是个“动态开关”,而非“静态锁”
研究团队提出并验证了一个关键假说:MHC-I分子在执行功能时,会经历一个**开放(open)和闭合(closed)的构象转换过程**。
- 开放态
肽结合槽打开,允许肽段进入或离开。 - 闭合态
肽结合槽关闭,形成稳定的复合物,准备呈递到细胞表面。
通过建立计算系统模型并拟合体内实验数据,他们发现:B*4405的“闭合速率”远快于B*4402。这意味着B*4405能更快地“锁住”一个肽段,然后通过其“开放速率”(该速率由肽段亲和力决定)来测试这个肽段的好坏。如果亲和力低(开放快),就迅速释放,再去尝试下一个;如果亲和力高(开放慢),就能稳定下来。这种快速的“试错-锁定”循环,使其筛选效率极高。而B*4402由于闭合太慢,整个筛选过程变得异常低效。
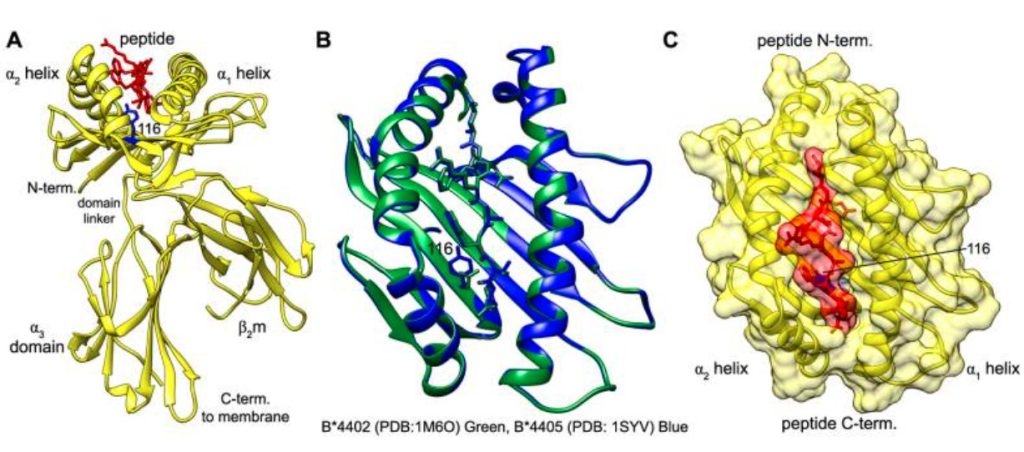
此图描述了三个特点(A、B、C),展示了: A-MHC I分子(HLA-B44:05)的整体结构及其组成; B-两个极其相似的等位基因(B4402 vs B4405)仅因一个氨基酸(116位)不同而产生功能差异(如影响T细胞识别或自身免疫反应); C-肽结合槽的结构特征,这是MHC I呈递抗原的关键部位。
上图呈现如下:
- (A)部分:
带状图”(ribbon diagram)展示蛋白质的三维结构,突出其二级结构(如α螺旋、β折叠)。
MHC I molecule HLA-B44:05:这是人类MHC I类分子的一种亚型,属于HLA-B基因座的一个等位基因产物(HLA是人类的MHC)。
共有三个组成部分:
Polymorphic heavy chain(多态性重链):MHC I类分子的α链,具有高度多态性(不同个体间序列差异大),决定抗原结合特异性。图中为黄色。
Invariant β2m(恒定的β2微球蛋白):即β₂-微球蛋白(β₂-microglobulin),不具多态性,与重链非共价结合,对MHC I分子稳定表达至关重要。图中也标为黄色(可能与重链同色,但实际是不同蛋白)。
Peptide(肽段):被MHC I呈递的抗原肽,通常为8–10个氨基酸长,来自细胞内降解的蛋白质(如病毒蛋白)。图中为红色。
Polymorphic residue 116:指在HLA-B44:02和HLA-B44:05这两个非常相似的等位基因之间,第116位氨基酸不同(这是它们的主要区别)。该残基位于肽结合槽底部,影响肽的选择和T细胞识别。图中用蓝色标出。 - (B)部分:
这是在比较两个高度相似的HLA-B44亚型的晶体结构:
B4402:来自PDB数据库编号 1M6O,图中绿色。
B4405:来自PDB编号 1SYV,图中蓝色。
RMSD = 0.3 Å:RMSD(Root Mean Square Deviation,均方根偏差)是衡量两个结构相似度的指标。0.3埃(Å)是非常小的差异(1 Å = 0.1 纳米),说明这两个分子的整体三维结构几乎完全相同,仅在个别残基(如116位)有差异。 - (C)部分:
这是MHC I分子肽结合槽(peptide-binding groove) 的混合展示方式:
Ribbon:显示蛋白质骨架的二级结构。
Surface:显示分子表面(通常是静电势或形状),突出肽结合槽的凹槽形状。
肽结合槽由重链的α1和α2结构域构成,像一个“沟”,中间容纳抗原肽。这个区域的多态性决定了能结合哪些肽。
分子动力学模拟:看见“柔性”的力量
为了从物理层面解释“闭合速率”的差异,研究团队进行了长达420纳秒的分子动力学(MD)模拟。
模拟结果显示,在**没有肽段结合**的状态下:
- B*4405
表现出高度的“可塑性”,其肽结合槽(F-pocket)能探索多种不同的构象,整体分子呈现出一种协调的“扭转”运动。 - B*4402
构象变化范围非常有限,显得僵硬而迟钝。
**结论一目了然:MHC-I分子的内在“柔性”(可塑性)直接决定了其构象转换(闭合)的速率,进而决定了其抗原选择功能的强弱。**
更令人信服的是,研究者通过定点突变(W147A)人为降低了B*4405的柔性,结果其抗原选择功能果然变得和B*4402一样差,完美验证了这一机制。
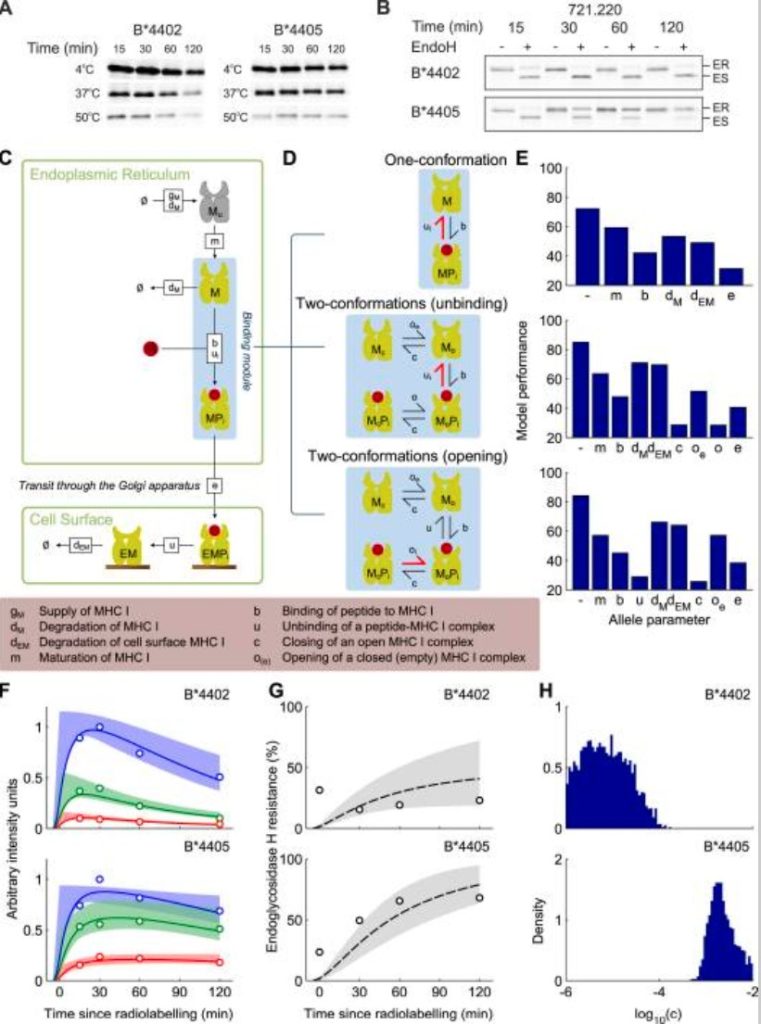
上图的意思是:
(A) 图 时间依赖的肽选择(通过脉冲追踪 + 热稳定性检测)
- 方法:用放射性同位素³⁵S-甲硫氨酸对tapasin缺失的721.220细胞进行5分钟脉冲标记,然后在不同时间点“追踪”(chase)。
- 细胞裂解后,将样品加热到不同温度(4°C、37°C、50°C),只有结合了高亲和力肽的MHC I才能耐受高温而不解聚。
- 目的:通过热稳定性间接反映MHC I所结合肽的亲和力随时间的变化。
- 结果量化见(F)。
(B) 图 MHC I向细胞表面转运的动力学(通过EndoH抗性测定)
- EndoH(内切糖苷酶H):只能切割未经过高尔基体修饰的N-糖链。因此:
- EndoH敏感(ES) → MHC I还在内质网或顺面高尔基体前(未成熟)。
- EndoH抗性(ER) → MHC I已通过顺面高尔基体,正在/已到达细胞表面(成熟)。
- 使用抗体W6/32免疫沉淀MHC I,并检测其EndoH抗性比例,从而推断MHC I离开内质网、转运到表面的速度。
- 特别说明:实验设计只捕获结合了高亲和力肽的MHC I(因W6/32只识别正确折叠且肽结合稳定的MHC I)。
- 结果量化见(G)。
(C) 图 无tapasin条件下肽选择的计算系统模型
- 用计算模型模拟MHC I在内质网中如何自主选择肽。
- 图中:
- 形状(shapes):代表不同分子状态(如空载MHC I、肽-MHC复合物等)。
- 带标签的方框:代表化学反应步骤(如肽结合、MHC构象变化),并标有速率参数(如结合速率k_on、解离速率k_off等)。
(D)图 两种可能的结合机制模型
- 单构象模型(one-conformation):假设MHC I只有一个构象状态,肽直接结合。
- 双构象模型(two-conformation):假设MHC I可在“开放”(open,易结合肽)和“闭合”(closed,稳定肽-MHC)之间转换。
- 红色粗线/符号:表示肽依赖的反应步骤(即只有在肽存在时才发生,如MHC从开放变为闭合)。
(E) 图 模型比较与最优模型选择
- 使用贝叶斯信息准则(BIC) 比较不同模型的拟合优度(BIC越低越好)。
- 最优模型:双构象模型,其中:
- 肽依赖的步骤是MHC I的“打开”(opening);
- 等位基因特异性参数是“闭合速率c”(即不同HLA等位基因关闭速度不同,影响肽选择效率)。
(F) 图 实验 vs 模型模拟:热稳定性数据
- 圆圈:来自(A)的实验数据(不同温度下剩余MHC I比例)。
- 实线:最优模型的模拟结果。
- 颜色含义:
- 蓝色(4°C):所有MHC I(无论肽亲和力高低)都稳定。
- 绿色(37°C):中+高亲和力肽-MHC复合物稳定。
- 红色(50°C):仅高亲和力肽-MHC复合物稳定。
- 阴影区域:95%置信区间,反映模型不确定性。
(G) 图 实验 vs 模型模拟:细胞表面转运(EndoH抗性)
- 圆圈:来自(B)的EndoH抗性百分比(即已转运出内质网的MHC I比例)。
- 实线:模型预测的转运动力学。
- 同样显示模型能很好地拟合实验数据。
(H) 图等位基因特异性闭合速率c的后验概率分布
- 使用贝叶斯推断,根据实验数据反推参数“c”(MHC I闭合速率)的可能取值。
- 横轴:闭合速率c的数值。
- 纵轴:该值在给定数据和模型下的后验概率密度。
- 峰值位置表示最可能的c值,宽度反映不确定性。
- 不同等位基因(如HLA-B44:02 vs B44:05)会有不同的c值,解释其肽选择效率差异。
- 即使在没有tapasin的情况下,MHC I仍能通过自身构象动态(开放↔闭合)选择高亲和力肽;
- 不同HLA等位基因的差异主要体现在闭合速率(c) 上——这决定了它们“锁定”合适肽的速度;
- 双构象模型比传统单构象模型更能解释实验观察到的肽选择和转运动力学;
- 这一机制可解释为何某些HLA等位基因(如B44:02 vs B44:05)在免疫应答或疾病易感性上表现不同。
参考文献: Selector function of MHC I molecules is determined by protein plasticity. Sci Rep. 2015.
如何将转化为研究成果?
桂芎生物可提供关键产品支撑:
1. 微量pMHC复合物合成服务: 支持HLA-A*02:01等33种主流HLA等位基因,用于抗原特异性T细胞验证
2 . pMHC荧光四聚体合成以及筛选: 现货覆盖多种肿瘤抗原(如HPV/CMV/EBV/KRAS等),快速分选抗原特异性T细胞
3. 工程化呈递细胞构建: K562-HLA系列,模拟体内抗原呈递,用于DC功能模拟
4. 单克隆TCR测序: 从四聚体阳性T细胞中获取配对链的TCR主克隆
5. 抗原肽-MHC亲和力高通量ELISA扫描服务: 高通量筛选最优表位,指导DC疫苗设计
6. 抗原特异性T细胞扩增: 桂芎拥有稳定的抗原特异性DC的分化成熟工艺,是抗原特异性T细胞扩增和检测的基石。
点击网页右侧”快速联系人“扫码,获取服务方案 + 成功案例.
Views: 12
