研究揭示,一个名为V2的T细胞模拟抗体(TCRm),通过形成一个由疏水氨基酸构成的“笼子”,精准捕获并识别KRAS G12V突变产生的新抗原肽。 KRAS G12V是胰腺癌、肺癌等“癌王”的常见驱动突变,但因其位于细胞内,传统抗体药物难以触及。 免疫疗法提供了一条新路:利用T细胞来识别由HLA分子呈递到细胞表面的KRAS G12V突变肽段(新抗原)。然而,如何让T细胞或其工程化产物(如TCR-T、双特异性抗体)精准区分“突变”与“野生型”(仅一个氨基酸之差),是巨大的挑战。近日,约翰霍普金斯大学团队在《Nature Communications》上发表重磅研究,首次利用冷冻电镜(cryo-EM)技术,从原子层面揭示了这一精准识别的奥秘——疏水作用力(Hydrophobic Interactions)。
突破:看清“导弹”与“靶标”的原子级对接
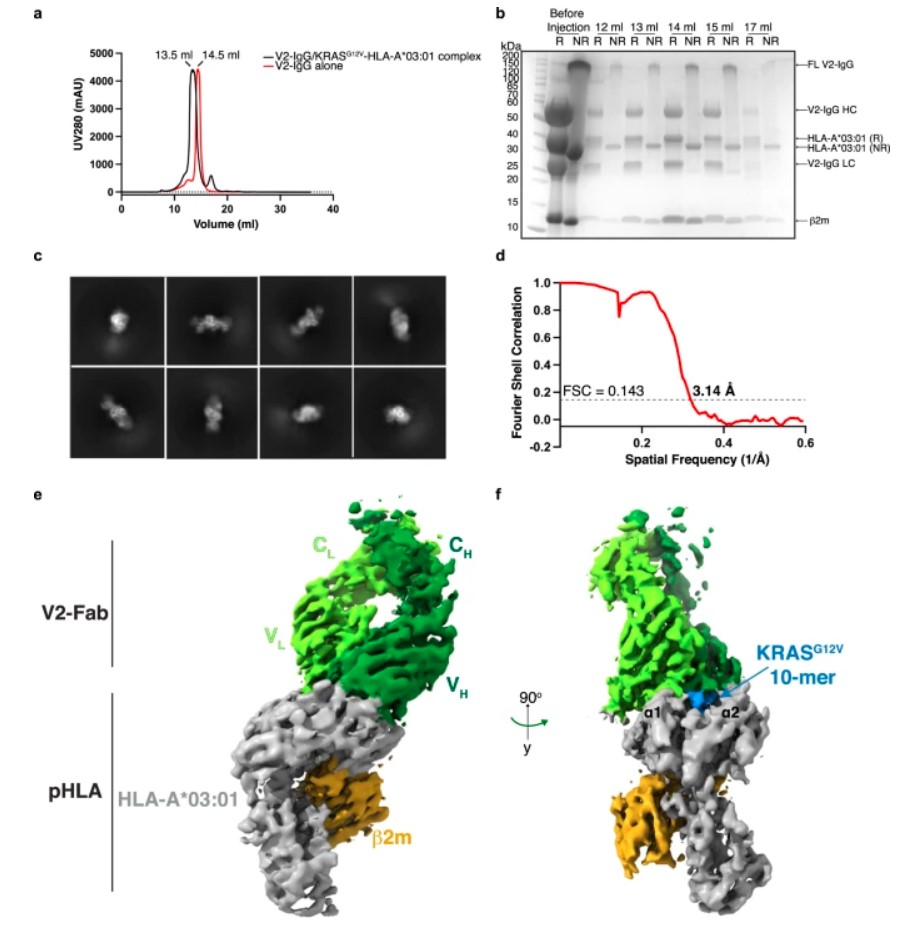
研究团队聚焦于一种名为V2的T细胞受体模拟抗体(TCR mimic, TCRm)。这是一种能像T细胞一样识别HLA-新抗原复合物的工程化抗体。他们成功解析了V2抗体与KRAS G12V肽段-HLA-A*03:01复合物的高分辨率(3.14 Å)冷冻电镜结构。
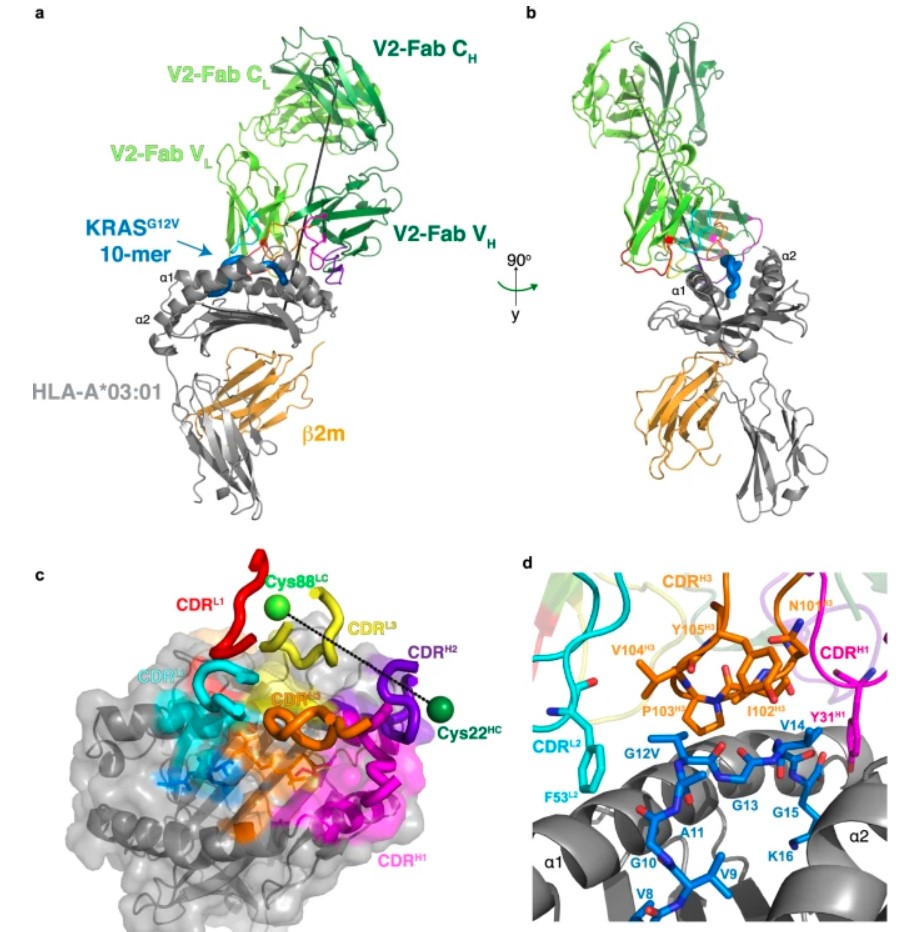
结构显示,V2抗体并非全面覆盖整个肽段,而是**高度倾斜地“坐”在肽段的C端**,其互补决定区(CDR)环,特别是CDR H3,直接对准了关键的G12V突变位点。
核心机制:一个精巧的“疏水笼子”
最令人惊叹的发现是识别的化学本质。V2抗体的CDR H3和CDR L2区域的几个关键氨基酸(Pro103H3, Val104H3, Tyr105H3, Phe53L2)共同构成了一个**松散的疏水性“笼子”**。
- 对于G12V突变体
突变产生的缬氨酸(Valine)是一个**疏水性**氨基酸。它恰好能被这个“疏水笼子”完美包裹,通过强大的疏水作用力实现稳定结合。 - 对于野生型G12
野生型是甘氨酸(Glycine),它**没有侧链**,无法与这个疏水笼子形成任何有效的相互作用,因此无法被有效识别。
这一机制解释了V2抗体为何能实现惊人的特异性——**不是靠识别突变带来的新化学基团,而是靠识别突变带来的“疏水性”**。
意外收获:抗体还能“诱导契合”
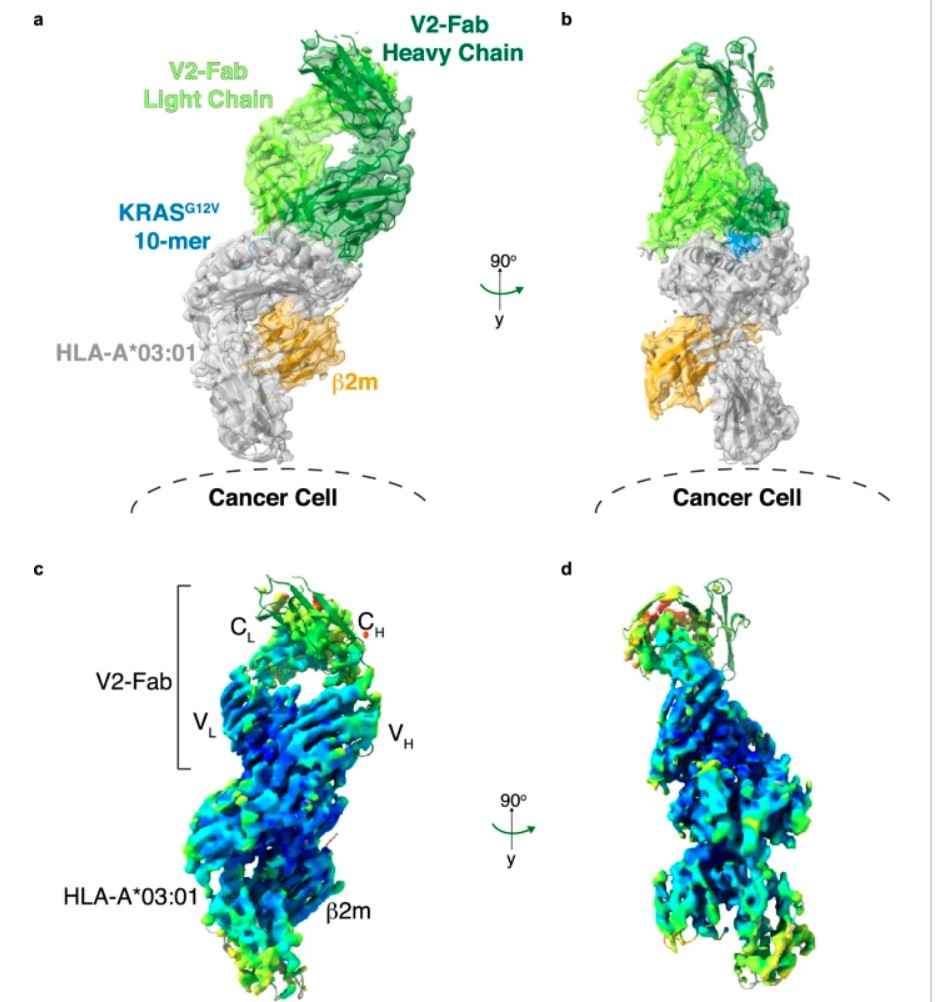
研究还有另一项重要发现。通过比较V2抗体结合前后的KRAS G12V肽段结构,他们发现V2的结合**诱导了肽段发生显著的构象变化**(Induced Fit)。
在未结合状态下,肽段相对平直;而一旦V2抗体结合,肽段的C端(特别是Lys16)会被推得更深地嵌入HLA的结合槽中,从而带动整个肽段发生N端位移。这种动态的“诱导契合”过程,进一步增强了V2对抗原的特异性识别能力。
启示:为“不可成药”靶点设计精准武器
这项研究的意义远不止于KRAS G12V本身。它提供了一个清晰的设计蓝图:对于由**疏水性突变**(如G12V, G12C)产生的新抗原,可以优先考虑设计能够形成**疏水口袋或笼子**的TCR或TCRm抗体。同时,研究也提醒我们,在抗体工程化改造(亲和力成熟)过程中,必须谨慎行事。文中尝试的多个突变虽然提高了体外结合力,却未能提升甚至损害了T细胞功能,凸显了**功能验证**的不可或缺性。
未来,结合结构生物学指导的理性设计与高通量的功能筛选,将是攻克KRAS等“不可成药”靶点的关键。
总结而言,这项来自顶尖团队的研究,如同一次精妙的“分子拆弹”,在原子尺度上揭示了免疫系统如何精准识别癌细胞的“身份密码”。这不仅加深了我们对基础免疫学的理解,更为开发下一代更安全、更有效的T细胞疗法铺平了道路。
参考文献:Hydrophobic interactions dominate the recognition of a KRAS G12V neoantigen. Nature Communications, 2023
如何将转化为研究成果?
桂芎生物可提供关键产品支撑:
1. 微量pMHC复合物合成服务: 支持HLA-A*02:01等33种主流HLA等位基因,用于抗原特异性T细胞验证
2 . pMHC荧光四聚体合成以及筛选: 现货覆盖多种肿瘤抗原(如HPV/CMV/EBV/KRAS等),快速分选抗原特异性T细胞
3. 工程化呈递细胞构建: K562-HLA系列,模拟体内抗原呈递,用于DC功能模拟
4. 单克隆TCR测序: 从四聚体阳性T细胞中获取配对链的TCR主克隆
5. 抗原肽-MHC亲和力高通量ELISA扫描服务: 高通量筛选最优表位,指导DC疫苗设计
6. 抗原特异性T细胞扩增: 桂芎拥有稳定的抗原特异性DC的分化成熟工艺,是抗原特异性T细胞扩增和检测的基石。
点击网页右侧”快速联系人“扫码,获取服务方案 + 成功案例.
Views: 11
